Что такое коррозия
С течением времени металлическое оборудование стареет и разрушается из-за коррозионных процессов. В Российской Федерации ежегодные потери металлов составляют до 12% от общей массы металлофонда, что соответствует утрате до 30% металла ежегодно. [1]
Что же такое коррозия?
Основные понятия и термины, относящиеся к коррозии металлов, приведены в «ГОСТ 5272-68. Коррозия металлов. Термины». Рассмотрим несколько основных понятий.
Коррозия металлов - разрушение металлов вследствие химического или электрохимического взаимодействия их с коррозионной средой.
Коррозионная среда - среда, в которой происходит коррозия металла.
Коррозионная стойкость - способность металла сопротивляться коррозионному воздействию среды.
Есть много способов классифицировать коррозию, но для лучшего понимания процесса остановимся на классификации по механизму протекания. По данному параметру коррозию делят на химическую и электрохимическую.
Химическая коррозия
Химическую коррозию рассмотрим не так подробно, так как коррозия по данному механизму редко встречается в природе, однако часто встречается в различных технологических процессах, где имеют место высокие температуры и сухая среда. По химическому механизму металл корродирует при отсутствии влаги или любой другой токопроводящей среды.
Металл выполняет роль восстановителя, в то время как коррозионная среда выступает в роли окислителя.
В качестве примера такой реакции рассмотрим реакцию железа с хлором.
![]()
В результате данной реакции на поверхности железа образуется плёнка из хлорида железа. В промышленности подобная реакция реализуется при получении соляной кислоты, поскольку аппараты изготавливают из стали. Пример данного вида коррозии можем увидеть на рисунке 1.
Рисунок 1 – Утилизация баллонов из-под хлора
Электрохимическая коррозия
Электрохимическая коррозия – это разрушение металлов в токопроводящих средах. Токопроводящую среду называют электролитом, а металл погруженный в электролит электродом. Электролитом может являться влага в воздухе, различные растворы щелочей, солей, кислот, почва, утренняя роса. Коррозия, с которой мы встречаемся каждый день, – это именно электрохимическая коррозия.
Рисунок 2 – Крышка, подвергшаяся электрохимической коррозии
Рассмотрим подробнее этот механизм на примере стальной конструкции, стоящей на открытом воздухе. В воздухе так или иначе присутствует влага, выпадают дожди, образуется роса – всё это создаёт на поверхности металла токопроводящую среду. В результате на поверхности металла образуются ионы, которые вступают в реакцию с кислородом образуя бурый налёт – ржавчину. Из-за перехода ионов в раствор на поверхности металла возникает электрический ток, который называют электродным потенциалом.
Рисунок 3 – Возникновение электрохимического потенциала
Электродный потенциал позволяет оценить влияние различных факторов среды на металл. Электродные потенциалы различных металлов заметно различаются. Чем меньше электродный потенциал металла, тем выше его химическая активность, а значит меньше его стойкость в агрессивных средах. Стандартные электродные потенциалы некоторых металлов приведены в таблице 1. Из таблицы видно, что наиболее охотно взаимодействует со средой алюминий, а наиболее стойко к воздействиям среды золото.
Таблица 1 – Стандартные электродные потенциалы металлов
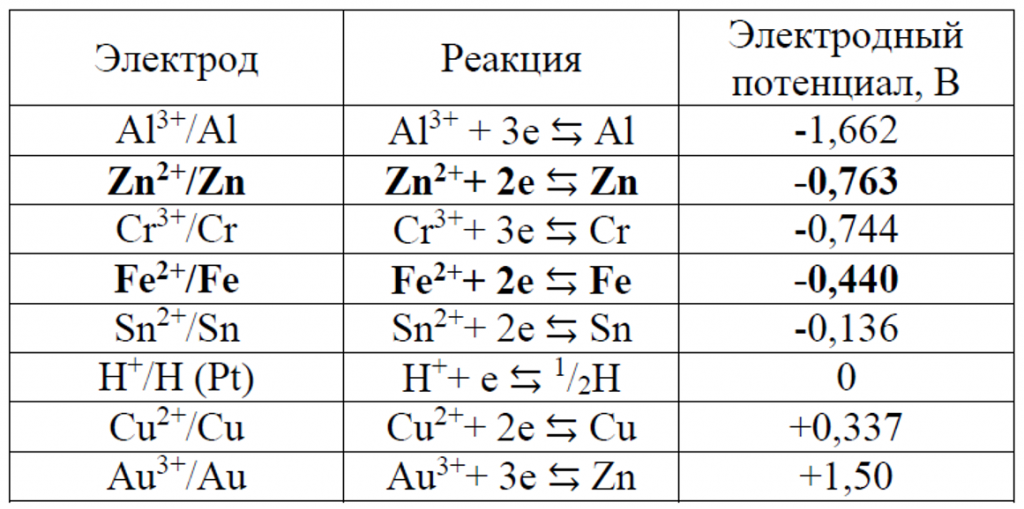
На интенсивность процесса коррозии, помимо природы металла так же влияет состав электролита. Например, на чистом воздухе металлическая конструкция будет корродировать медленней, чем в воздухе промзоны или морского побережья. Это связано с тем, что в воздухе промышленных зон содержатся различные соединения серы, которые своим воздействием увеличивают интенсивность коррозии.
Рисунок 4 – Коррозия в промышленной зоне
Рисунок 5 – Коррозия в морском климате
Также на коррозию влияет температура, при которой эксплуатируется конструкция. При повышении температуры скорость коррозии увеличивается.
Поэтому при выборе способа защиты от коррозии необходимо принимать во внимание условия среды, где будет стоять и как будет эксплуатироваться конструкция.
-
Семёнова И.В., Флорианович Г.М., Хорошилов А.В. / Коррозия и защита от коррозии: Учеб. пособие. – М.:Физматлит, 2002. – 336 с.
-
ГОСТ 5272-68. Коррозия металлов. Термины.
-
Авдеенко А.П., Поляков А.Е., Юсина А.Л. / Коррозия и защита металлов. Справочное пособие. – Краматорск: ДГМА, 2004. – 112с



